DBV s'envole de 14% avant une nouvelle demande à la FDA pour Viaskin Peanut
February 14 2019 - 3:53AM
Bourse Web Dow Jones (French)
PARIS (Agefi-Dow Jones)--DBV Technologies s'envole de 14% à 14,14
euros jeudi matin, après avoir annoncé mercredi soir son intention
de soumettre au troisième trimestre une nouvelle demande
d'autorisation de mise sur le marché (Biologics Licence Application
ou "BLA") à l'autorité sanitaire américaine, la Food and Drug
Administration (FDA), pour son produit Viaskin Peanut dans le
traitement des enfants de 4 à 11 ans allergiques à l'arachide. La
société de biotechnologies avait retiré en décembre sa précédente
demande d'autorisation pour Viaskin Peanut, après des échanges avec
la FDA concernant des demandes de données complémentaires sur les
procédures de fabrication et les contrôles qualité. "Nous avons
considérablement progressé dans la prise en compte des demandes
d'informations requises pour une nouvelle soumission de notre BLA à
la suite des commentaires que la FDA nous a adressés en décembre
2018", a déclaré Daniel Tassé, directeur général de DBV
Technologies, cité dans un communiqué. (fberthon@agefi.fr) ed:
VLV
Agefi-Dow Jones The financial newswire
(END) Dow Jones Newswires
February 14, 2019 03:33 ET (08:33 GMT)
Copyright (c) 2019 L'AGEFI SA
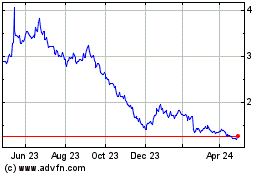
DBV Technologies (EU:DBV)
Historical Stock Chart
From Sep 2024 to Oct 2024
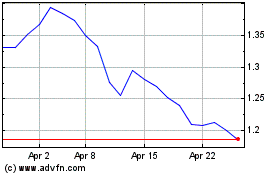
DBV Technologies (EU:DBV)
Historical Stock Chart
From Oct 2023 to Oct 2024