Erste Ergebnisse aus dem Sicherheitseinlauf der
Phase-3-Studie LOTIS-5 zeigen eine ORR von 75 % und eine CR-Rate
von 40 % ohne neue Sicherheitssignale
Zulassungsrelevante Phase-2-Daten zu Cami
werden in zusätzlichen mündlichen und Posterpräsentationen in den
Blickpunkt gerückt
ADC Therapeutics SA (NYSE: ADCT) gab heute bekannt, dass
Abstracts zu ZYNLONTA® (Loncastuximab-Tesirin-Lpyl) und
Camidanlumab-Tesirin (Cami) für die Präsentation auf der 10.
Jahrestagung der Society of Hematologic Oncology (SOHO 2022)
angenommen wurden, die vom 28. September bis 1. Oktober 2022 in
Houston, Texas/USA stattfindet.
„Wir freuen uns darauf, auf der SOHO 2022 die ermutigenden
ersten Ergebnisse aus dem Sicherheitseinlauf unserer klinischen
Phase-3-Studie LOTIS-5 vorzulegen, mit der ZYNLONTA in Kombination
mit Rituximab bei Patienten mit rezidiviertem oder refraktärem
diffusem großzelligem B-Zell-Lymphom untersucht wurde“, erklärte
Dr. Joseph Camardo, Chief Medical Officer von ADC Therapeutics. „Es
handelt sich dabei um eine von mehreren klinischen Studien zu
ZYNLONTA in Kombination mit anderen Arzneimitteln, mit der ZYNLONTA
in früheren Behandlungslinien evaluiert wird.“
Erste Ergebnisse aus dem ersten
Sicherheitseinlauf von LOTIS-5
LOTIS-5 ist eine randomisierte, offene, zweiteilige, zweiarmige,
multizentrische Phase-3-Studie zu Loncastuximab-Tesirin in
Kombination mit Rituximab (Lonca-R) bei Patienten mit rezidiviertem
oder refraktärem diffusem großzelligem B-Zell-Lymphom (DLBCL).
Zwanzig Patienten nahmen in Teil 1 an einem nicht-randomisierten
Sicherheitseinlauf teil. In Teil 2 werden ca. 330 Patienten im
Verhältnis 1:1 randomisiert und erhalten entweder Lonca-R oder
Rituximab-Gemcitabin-Oxaliplatin (R-GemOx).
Die 20 Teilnehmer des Sicherheitseinlaufs waren median 74,5
Jahre alt (Bereich 35 - 93 Jahre) und hatten median 1 frühere
Therapie erhalten (Bereich 1 - 6). Datenstichtag war der 28.
Februar 2022:
- Die Gesamtansprechrate lag gemäß einer zentralen Prüfung bei
15/20 (75 %). Insgesamt erzielten 8/20 (40 %) bzw. 7/20 (35 %) der
Patienten ein komplettes bzw. teilweises Ansprechen.
- Die häufigsten behandlungsbezogenen unerwünschten Reaktionen
(TEAE) aller Grade, unabhängig von ihrer Beziehung zur
Studienbehandlung, waren Hautausschlag (5 [25 %]), Müdigkeit (4 [20
%]) und erh�hte Gamma-Glutamyltransferase-Werte (4 [20 %]). Die
häufigsten TEAE Grad 3 oder h�her waren erh�hte
Gamma-Glutamyltransferase-Werte (3 [15 %]), erh�hte
Alanin-Aminotransferase-Werte (2 [10 %]) und Neutropenie (2 [10
%]).
Diese Daten werden auf dem folgenden Poster präsentiert:
Initial Safety Run‐In Results of the Phase 3 LOTIS‐5 Trial:
Novel Combination of Loncastuximab Tesirine With Rituximab
(Lonca‐R) Versus Immunochemotherapy in Patients With R/R DLBCL
Poster-Nummer: ABCL-320
Angaben zu den weiteren Posterpräsentationen von ADC
Therapeutics:
A Phase 2, Open-Label Study of Loncastuximab Tesirine in
Combination with Rituximab (Lonca-R) in Previously Untreated
Unfit/Frail Patients with Diffuse Large B-cell Lymphoma (DLBCL)
(LOTIS-9) (Zusätzliche Daten, erstmals als Präsentation)
Poster-Nummer: ABCL-272
Health-Related Quality of Life and Tolerability in Patients
With/Without Skin Toxicity During Loncastuximab Tesirine Treatment
in a Phase 2 Clinical Trial (LOTIS-2) Poster-Nummer:
ABCL-316
Long-term survival projections of loncastuximab
tesirine-treated patients in relapsed or refractory (R/R) diffuse
large B-cell lymphoma (DLBCL) (Zusätzliche Daten, erstmals als
Präsentation) Poster-Nummer: ABCL-334
Camidanlumab Tesirine: Updated Efficacy and Safety in an
Open-Label, Multicenter, Phase 2 Study of Patients with Relapsed or
Refractory Classical Hodgkin Lymphoma (R/R cHL) (Encore)
Poster-Nummer: HL-339
Alle Poster werden am Mittwoch, den 28. September von 17.05 bis
18.30 Uhr CT im Ballroom of Americas in der 2. Etage des
Hilton-Americas Houston präsentiert. Die Poster k�nnen auch am
Donnerstag und Freitag im Verlauf des Tages in der Posterhalle
eingesehen werden. Der Online-Zugriff auf die Poster beginnt für
angemeldete Kongressteilnehmer am Donnerstag, den 29.
September.
Angaben zu mündlichen Vorträgen von ADC Therapeutics:
Camidanlumab Tesirine: Updated Efficacy and Safety in an
Open-Label, Multicenter, Phase 2 Study of Patients with Relapsed or
Refractory Classical Hodgkin Lymphoma (R/R cHL) (Encore) Datum
und Uhrzeit: Freitag, 30. September, 17.48 - 17.58 Uhr CT Ort:
Grand Ballroom G-L, 4. Etage Referent: Dr. Alex Herrera, City of
Hope, Duarte, Kalifornien, USA Session XII: Hodgkin-Lymphom
Über ZYNLONTA® (Loncastuximab-Tesirin-Lpyl)
ZYNLONTA® ist ein auf CD19 abzielendes
Antik�rper-Wirkstoff-Konjugat (AWK). Sobald es an eine CD19
exprimierende Zelle gebunden ist, wird ZYNLONTA von der Zelle
internalisiert, wo Enzyme eine Pyrrolobenzodiazepin-Nutzlast (PBD)
freisetzen. Die hochwirksame Nutzlast bindet sich mit geringer
Verzerrung an die kleine DNA-Furche und bleibt dadurch weniger
sichtbar für die DNA-Reparaturmechanismen. Damit wird letztlich der
Zellzyklus gestoppt, und die Tumorzellen sterben ab.
Die US-amerikanische Arzneimittelbeh�rde FDA erteilte ZYNLONTA
(Loncastuximab-Tesirin-Lpyl) die Zulassung für die Behandlung
erwachsener Patienten mit rezidiviertem oder refraktärem (r/r)
großzelligem B-Zell-Lymphom nach zwei oder mehr Linien systemischer
Therapie, einschließlich des nicht anderweitig spezifizierten
DLBCL, sowie DLBCL, das aus einem niedriggradigen Lymphom entsteht,
und des hochgradigen B-Zell-Lymphoms. An der Studie nahm ein
breites Spektrum stark vorbehandelter Patienten (median drei
frühere Therapielinien) mit sehr schwer behandelbarer Erkrankung
teil, darunter Patienten, die auf die Erstlinientherapie nicht
ansprachen, Patienten, die bei allen vorherigen Therapielinien
refraktär waren, Patienten mit Double/Triple-Hit-Genetik und
Patienten, die vor ihrer Behandlung mit ZYNLONTA eine
Stammzelltransplantation und CAR-T-Therapie erhielten. Diese
Indikation wurde von der FDA aufgrund der Gesamtansprechrate im
beschleunigten Verfahren zugelassen, und die weitere Zulassung für
diese Indikation kann von der Überprüfung und Beschreibung des
klinischen Nutzens in einer Bestätigungsstudie abhängig gemacht
werden.
ZYNLONTA wird außerdem in Kombinationsstudien als Therapieoption
für andere B-Zell-Malignome und in früheren Therapielinien
evaluiert.
Über Camidanlumab-Tesirin (Cami)
Camidanlumab-Tesirin (Cami) ist ein
Antik�rper-Wirkstoff-Konjugat (AWK), das aus einem monoklonalen
Antik�rper besteht, der an CD25 (HuMax®-TAC, lizenziert von Genmab
A/S), bindet und mit der Pyrrolobenzodiazepin (PBD)-Dimer-Payload
Tesirin konjugiert ist. Sobald es an eine CD25-exprimierende
Tumorzelle gebunden ist, wird Cami in die Zelle internalisiert, wo
Enzyme die PBD-basierte Ladung (Payload) freisetzen und die Zelle
abt�ten. Dies gilt sowohl für CD25-exprimierende Tumorzellen als
auch für CD25-exprimierende regulatorische T-Zellen (Treg). Die
intratumorale Freisetzung der PBD-Payload kann auch zum
„Bystander-Killing“ benachbarter Tumorzellen führen. Außerdem wurde
gezeigt, dass PBD den immunogenen Zelltod induzieren. Alle diese
Eigenschaften von Cami k�nnen die immunvermittelte
Antitumoraktivität verbessern.
Cami wird in einer zulassungsrelevanten klinischen
Phase-2-Studie an Patienten mit rezidiviertem oder refraktärem
Hodgkin-Lymphom (HL) sowie in einer klinischen Phase-1b-Studie als
Monotherapie und in Kombination mit Pembrolizumab bei soliden
Tumoren untersucht.
Über ADC Therapeutics
ADC Therapeutics (NYSE: ADCT) ist ein kommerziell tätiges
Biotechnologieunternehmen, das mit seinen zielgerichteten
Antik�rper-Wirkstoff-Konjugaten (AWK) der nächsten Generation die
Lebensqualität von Krebspatienten verbessert. Das Unternehmen
treibt die Entwicklung seiner proprietären PBD-basierten
AWK-Technologie voran, um das Behandlungsparadigma für Patienten
mit hämatologischen Malignomen und soliden Tumoren zu
verändern.
Das auf CD19 abzielende AWK ZYNLONTA
(Loncastuximab-Tesirin-Lpyl) von ADC Therapeutics ist von der FDA
für die Behandlung des rezidivierten oder refraktären diffusen
großzelligen B-Zell-Lymphoms nach zwei oder mehr Linien
systemischer Therapie zugelassen. ZYNLONTA befindet sich auch als
Kombinationstherapie mit anderen Wirkstoffen in der Entwicklung.
Cami (Camidanlumab-Tesirin) bei rezidiviertem oder refraktärem
Hodgkin-Lymphom wird derzeit in einer zulassungsrelevanten
klinischen Phase-2-Studie und bei verschiedenen fortgeschrittenen
soliden Tumoren in einer klinischen Phase-1b-Studie evaluiert.
Neben ZYNLONTA und Cami hat ADC Therapeutics gegenwärtig mehrere
AWK in klinischer und präklinischer Entwicklung.
ADC Therapeutics mit Sitz in Lausanne (Biopôle), Schweiz, ist in
London, der San Francisco Bay Area und New Jersey tätig. Weitere
Informationen finden Sie unter https://adctherapeutics.com/. Folgen
Sie dem Unternehmen auch auf Twitter und LinkedIn.
ZYNLONTA® ist eine eingetragene Marke von ADC Therapeutics
SA.
Die Ausgangssprache, in der der Originaltext ver�ffentlicht
wird, ist die offizielle und autorisierte Version. Übersetzungen
werden zur besseren Verständigung mitgeliefert. Nur die
Sprachversion, die im Original ver�ffentlicht wurde, ist
rechtsgültig. Gleichen Sie deshalb Übersetzungen mit der originalen
Sprachversion der Ver�ffentlichung ab.
Originalversion auf businesswire.com
ansehen: https://www.businesswire.com/news/home/20220921005890/de/
Investorenkontakt Eugenia Litz ADC Therapeutics
Eugenia.Litz@adctherapeutics.com +44 7879 627205
Amanda Hamilton ADC Therapeutics
amanda.hamilton@adctherapeutics.com +1 917-288-7023
Medienkontakt Mary Ann Ondish ADC Therapeutics
maryann.ondish@adctherapeutics.com +1 914-552-4625
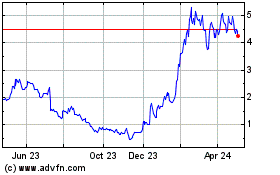
ADC Therapeutics (NYSE:ADCT)
Historical Stock Chart
From Mar 2024 to Apr 2024
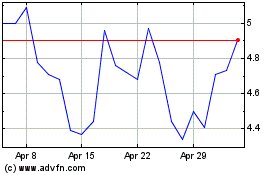
ADC Therapeutics (NYSE:ADCT)
Historical Stock Chart
From Apr 2023 to Apr 2024