Les ventes nettes de ZYNLONTA® (loncastuximab
tésirine-lpyl) au troisième trimestre 2021 ont atteint 13,1
millions USD
Un accord de financement a été signé avec
HealthCare Royalty pouvant aller jusqu'à 325 millions USD
La société organisera, aujourd'hui à 8:30 HAE,
une conférence téléphonique
ADC Therapeutics SA (NYSE: ADCT), une société biotechnologique
au stade commercial qui améliore la vie des personnes touchées par
le cancer grâce à ses conjugués anticorps-médicaments (CAM) ciblés
de nouvelle génération destinés aux patients présentant des
malignités hématologiques et des tumeurs solides, a communiqué
aujourd'hui ses résultats financiers du troisième trimestre clos au
30 septembre 2021. La société a également apporté des mises à jour
concernant ses activités.
"Nous sommes satisfaits de la dynamique du lancement de
ZYNLONTA® à ce jour et de l'accueil favorable que lui a réservé la
communauté des praticiens. La poursuite de la croissance de
ZYNLONTA ainsi que le développement de son potentiel au long terme
pour les patients demeurent nos principales priorités," a déclaré
Chris Martin, PhD, directeur général d'ADC Therapeutics. "Nous
sommes également très enthousiastes de constater les progrès
réalisés par notre portefeuille diversifié de stade clinique, à la
fois dans le domaine de l'hématologie et des tumeurs solides,"
a-t-il poursuivi.
Temps forts et évolutions
récentes
ZYNLONTA
- ZYNLONTA a généré des ventes nettes de 13,1 millions USD au
cours du troisième trimestre 2021, premier trimestre entier de
ventes.
- Les centres universitaires représentaient plus de 50% du volume
total avec un ratio d'environ 50-50 des comptes universitaires et
communautaires au troisième trimestre.
- La société a continué d'engager de nouveaux comptes et
d'accroître le volume des comptes existants et prioritaires, y
compris les centres du National Comprehensive Cancer Network
(NCCN).
- La sensibilisation, la perception et l'intention de
prescription, assistées et spontanées de la marque, ont poursuivi
leur hausse tout au long du trimestre.
- Le payeur bénéficie d'un accès plus large au traitement, sans
obstacle à ce jour. Un programme complet de soutien au patient et
un accompagnement progressif du patient sont disponibles.
- La société a continué de fonctionner efficacement dans le
contexte dynamique de la COVID. Les équipes de ventes et médicales
exécutent un modèle hybride réalisant à la fois des interactions
virtuelles et en face-à-face, selon les préférences des clients et
la situation locale.
Un portefeuille de stade clinique
- ADCT-901: Un premier patient a reçu une dose dans
l'étude de Phase 1 portant sur ADCT-901, ciblant KAAG-1, un nouvel
antigène exprimé dans de nombreux cancers, chez des patients
atteints de tumeurs solides avancées. KAAG-1 est exprimé de manière
intracellulaire dans les tissus sains, mais sa surexpression se
produit sur la membrane de certaines tumeurs solides avancées,
telles le cancer de l'ovaire et le cancer du sein, y compris le
cancer du sein triple négatif.
- ADCT-701: Une collaboration a été instaurée avec le
National Cancer Institute (NCI) des National Institutes of Health
en vue du développement continu de ADCT-701, ciblant le DLK-1, dans
les malignités neuroendocrines. Le DLK-1 est exprimé lors du
développement embryonnaire, mais son expression est
particulièrement limitée dans les tissus adultes sains. Sa
surexpression se produit sur la membrane de certaines tumeurs
solides avancées présentes dans le carcinome adrénocortical, le
phéochromocytome, le paragangliome, le neuroblastome et le cancer
du poumon à petites cellules.
Mise à jour d'entreprise
- Expansion géographique: ADC Therapeutics s'engage à
élargir son empreinte géographique pour fournir ZYNLONTA et
d'autres traitements novateurs aux patients susceptibles d'en tirer
profit, dans le monde entier.
- La demande d'autorisation de mise sur le marché (AMM) pour
ZYNLONTA a été validée en octobre par l'Agence européenne des
médicaments (EMA) pour son traitement chez les patients atteints de
lymphome diffus à grandes cellules B (LDGCB) récidivant ou
réfractaire.
- La désignation de médicament orphelin a été accordée à ZYNLONTA
dans l'UE pour le traitement du LDGCB.
- Overland ADCT BioPharma a dosé le premier patient dans le cadre
de l'essai clinique pivot de Phase 2 sur ZYNLONTA chez les patients
atteints de lymphome diffus à grandes cellules B (LDGCB) récidivant
ou réfractaire en Chine, qui vise à appuyer l'enregistrement
anticipé de ZYNLONTA dans ce pays.
Prochains jalons prévus
ZYNLONTA
- Lancement de l'étude établissant la posologie de ZYNLONTA dans
le traitement de première intention du LDGCB avec R-CHOP au
quatrième trimestre 2021.
- Lancement de l'étude clinique visant l'évaluation de ZYNLONTA
dans plusieurs combinaisons de traitement du lymphome
non-hodgkinien à grandes cellules B au quatrième trimestre
2021.
- Finalisation du recrutement pour l'essai d'innocuité de l'étude
confirmatoire LOTIS-5 de Phase 3 sur ZYNLONTA en association avec
rituximab au quatrième trimestre 2021.
- Poursuite du recrutement dans le cadre de l'étude LOTIS-3 de
Phase 2 sur ZYNLONTA en association avec ibrutinib au quatrième
trimestre 2021.
Cami
- Finalisation du suivi à 12 mois de l'essai de Phase 2 chez les
patients atteints de lymphome hodgkinien récidivant ou réfractaire
au premier trimestre 2022.
- Rapport des résultats préliminaires pour l'essai de Phase 2
chez les patients atteints de lymphome hodgkinien au premier
semestre 2022.
- Finalisation de la posologie dans le cadre de l'essai de Phase
1b sur les tumeurs solides en association avec pembrolizumab.
Un portefeuille de stade clinique
- Lancement d'une étude combinée de Phase 1b sur ADCT-601
(mipasetamab uzoptirine), dans le traitement des tumeurs connues
pour exprimer AXL, au premier semestre 2022.
Résultats financiers du troisième
trimestre 2021
Trésorerie et équivalents de trésorerie
Au 30 septembre 2021, la trésorerie et équivalents de trésorerie
s'élevaient à 530,2 millions USD, en comparaison avec 371,9
millions au 30 juin 2021. Au cours du troisième trimestre 2021, la
société a conclu un accord de financement avec HealthCare Royalty
Partners (HCR) d'un montant pouvant aller jusqu'à 325 millions USD,
y compris un produit brut de 225 millions USD à la clôture avant
déduction des coûts de transaction de 7,0 millions USD.
Produits d'exploitation
Les produits d'exploitation (nets) étaient de 13,1 millions USD
pour le trimestre clos au 30 septembre 2021, en comparaison avec
zéro à la même période l'année précédente (2020). Les recettes
annuelles nettes correspondent aux ventes de ZYNLONTA aux
Etats-Unis, qui ont bénéficié d'une procédure d'approbation
accélérée de la FDA le 23 avril 2021.
Dépenses de Recherche et de Développement (R&D)
Les dépenses de R&D étaient de 36,8 millions USD pour le
trimestre clos au 30 septembre 2021, en comparaison avec 32,2
millions USD pour la même période de l'année précédente (2020). Les
dépenses de R&D se sont accrues en raison d'investissements
dans des programmes évaluant le potentiel de ZYNLONTA dans des
lignes de traitement antérieures et histologies additionnelles, et
faisant progresser le portefeuille. En résultat de ces initiatives,
l'effectif et la rémunération en actions se sont accrus.
Dépenses de Ventes et de Marketing (V&M)
Au cours du troisième trimestre 2021, les dépenses de Ventes et
de Marketing s'élevaient à 17,0 millions USD en comparaison avec
6,1 millions USD pour le même trimestre de l'année précédente
(2020). L'augmentation des dépenses de V&M était liée au
lancement de ZYNLONTA. Avant le 31 décembre 2020, les dépenses de
V&M étaient enregistrées dans les dépenses générales et
administratives (G&A) dans l'état de résultats consolidé
condensé provisoire. La période close au 30 septembre 2020 a été
revue pour être conforme à la présentation de l'exercice en
cours.
Dépenses générales et administratives (G&A)
Les dépenses générales et administratives étaient de 16,6
millions USD pour le trimestre clos au 30 septembre 2021, en
comparaison à 14,2 millions USD pour la même période en 2020. Ces
dépenses se sont accrues en raison de l'augmentation des effectifs
dans le but d'appuyer le lancement commercial et d'accroître les
charges liées aux rémunérations en actions.
Pertes nettes et pertes nettes ajustées
Les pertes nettes s'élevaient à 71,5 millions USD, soit une
perte nette de 0,93 USD par action de base et diluée, pour le
trimestre clos au 30 septembre 2021, en comparaison avec 20,3
millions USD, soit une perte nette de 0,29 USD par action de base
et diluée, pour le même trimestre de l'année précédente (2020). Les
pertes nettes incluaient des charges de rémunération en actions de
14,8 millions USD pour le trimestre clos au 30 septembre 2021, en
comparaison avec 11,0 millions USD pour le même trimestre de
l'année précédente (2020). En outre, les pertes nettes pour le
trimestre clos au 30 septembre 2021 incluent une perte non
monétaire de 6,9 millions USD liée aux variations de juste valeur
des instruments dérivés associés aux emprunts convertibles en vertu
de la facilité de crédit convertible signée avec Deerfield, en
comparaison avec un gain non monétaire de 33,9 millions USD au même
trimestre de l'année précédente (2020). L'augmentation de la juste
valeur pour le trimestre clos au 30 septembre 2021 résultait de
l'augmentation du prix de l'action de la société à compter du 30
juin 2021. La diminution de la juste valeur au trimestre clos au 30
septembre 2020 résultait principalement de la diminution du prix de
l'action de la société à compter du 30 juin 2020.
La perte nette ajustée était de 45,6 millions USD, soit une
perte nette ajustée de 0,59 USD par action de base et diluée, pour
le trimestre clos au 30 septembre 2021, en comparaison avec 41,3
millions USD, soit une perte nette ajustée de 0,58 USD par action
de base et diluée, pour le même trimestre en 2020. L'augmentation
de la perte nette ajustée résultait principalement des
investissements dans le portefeuille clinique en expansion et du
lancement de ZYNLONTA.
Détails relatifs à la conférence téléphonique
La direction d'ADC Therapeutics organisera une conférence
téléphonique et un webinaire audio en direct pour débattre des
résultats financiers du troisième trimestre 2021 et fournir une
mise à jour de l'entreprise aujourd'hui à 8:30 Heure de l'Est des
Etats-Unis. Pour accéder à la conférence en direct, veuillez
composer le 833-303-1198 (aux Etats-Unis) ou le +1 914-987-7415 (à
l'international) et indiquer l'identifiant de la conférence:
4035885. Un webinaire en direct de la présentation sera disponible
dans le volet "Evénements et présentations" de la section
Investisseurs du site d'ADC Therapeutics à l'adresse
ir.adctherapeutics.com. Une fois archivé, le webinaire sera
disponible pendant les 30 jours suivant la conférence
téléphonique.
À propos de ZYNLONTA® (loncastuximab
tésirine-lpyl)
ZYNLONTA® est un conjugué anticorps-médicament (CAM) ciblant le
CD19. Une fois lié à une cellule exprimant le CD19, ZYNLONTA est
internalisé par la cellule, où des enzymes libèrent une charge
utile de pyrrolobenzodiazépine (PBD). Cette charge utile puissante
se lie au sillon mineur de l'ADN avec une faible distorsion,
demeurant ainsi moins visible pour les mécanismes de réparation de
l'ADN. Il en résulte au final un arrêt du cycle cellulaire et la
mort des cellules tumorales.
L'Agence américaine des produits alimentaires et médicamenteux
(FDA) a approuvé ZYNLONTA (loncastuximab tésirine-lpyl) pour le
traitement des patients adultes atteints d'un lymphome à grandes
cellules B récidivant ou réfractaire (r/r) à la suite d'au moins
deux lignes de traitement systémique, y compris le lymphome diffus
à grandes cellules B (LDGCB) non spécifié, le LDGCB issu d'un
lymphome de bas grade et le lymphome à grandes cellules B de haut
grade. L'essai comprenait un large éventail de patients lourdement
prétraités (en moyenne trois lignes de traitement antérieures)
présentant une maladie très difficile à traiter, y compris des
patients n'ayant pas répondu au traitement de première intention,
des patients réfractaires à toutes les lignes de traitement
antérieures, des patients avec événement génétique double/triple
hit et des patients ayant reçu des greffes de cellules souches et
suivi une thérapie CAR-T avant leur traitement par ZYNLONTA. Cette
indication est approuvée par la FDA dans le cadre d'une approbation
accélérée basée sur le taux de réponse globale, et le maintien de
l'approbation pour cette indication peut être subordonné à la
vérification et à la description du bénéfice clinique dans un essai
de confirmation.
ZYNLONTA fait également l'objet d'une évaluation en association
avec de précédentes lignes thérapeutiques et dans d'autres
affections malignes à cellules B.
À propos d’ADC Therapeutics
ADC Therapeutics (NYSE : ADCT) est une société biotechnologique
en phase commerciale améliorant la qualité de vie des personnes
atteintes de cancer grâce à ses conjugués anticorps-médicament
(CAM) ciblés de prochaine génération. La Société s'appuie sur sa
technologie CAM exclusive, basée sur les PBD, pour transformer le
paradigme thérapeutique pour les patients atteints d'affections
malignes hématologiques et de tumeurs solides.
Le CAM ZYNLONTA™ (loncastuximab tésirine-lpyl) ciblant le CD19
d'ADC Therapeutics est approuvé par la FDA pour le traitement du
lymphome diffus à grandes cellules B, récidivant ou réfractaire,
après au moins deux lignes de thérapies systémiques. ZYNLONTA fait
également l'objet d'essais cliniques en phase avancée en
association avec d'autres agents. Le camidanlumab tésirine (Cami)
est en cours d'évaluation dans un essai clinique en phase avancée
pour le lymphome hodgkinien récidivant ou réfractaire et dans un
essai clinique de Phase 1b pour diverses tumeurs solides avancées.
Outre le ZYNLONTA et le Cami, la Société dispose de multiples CAM
en cours de développement clinique et préclinique.
ADC Therapeutics est basée à Lausanne (Biopôle), en Suisse, et
exerce ses activités à Londres, dans la Baie de San Francisco et
dans le New Jersey. Pour de plus amples informations, veuillez
consulter https://adctherapeutics.com/ et suivez-nous sur Twitter
et LinkedIn.
ZYNLONTA® est une marque déposée d'ADC Therapeutics SA.
Utilisation d'indicateurs financiers non IFRS
En plus des informations financières préparées en accord avec
les IFRS, ce document contient également certains indicateurs
financiers non IFRS reposant sur l'interprétation, selon l'équipe
de direction, des performances mesurées, notamment:
- Perte nette ajustée par action
La direction utilise ce type de mesures en interne lors de la
surveillance et de l'évaluation de notre performance
opérationnelle, de la génération de plans opérationnels futurs et
de la prise de décisions stratégiques relatives à l'attribution de
capital. Nous croyons que ces mesures financières ajustées offrent
des informations utiles aux investisseurs et autres, qui leur
permettent de comprendre et d'évaluer nos résultats opérationnels
de la même façon que notre direction. Elles facilitent également la
comparaison entre les différentes performances opérationnelles, au
cours des périodes de déclaration à la fois passées et futures. Ces
mesures non IFRS comportent certaines limites en tant que mesures
financières. Elles doivent être considérées comme un complément des
informations préparées conformément aux IFRS, et non comme un
élément isolé ou substitut de celles-ci. Lors de la préparation de
ces mesures complémentaires non IFRS, la direction exclut
généralement certains postes qui, selon elle, ne sont pas
révélateurs de notre performance opérationnelle en cours. Elle ne
considère pas en outre ces postes IFRS comme des dépenses
opérationnelles monétaires récurrentes normales. Ces postes ne
correspondent cependant pas à la définition IFRS de postes
inhabituels ou non récurrents. Etant donné que les mesures
financières non conformes aux IFRS ne possèdent ni définition ni
signification normalisée, il est possible qu'elles diffèrent des
mesures non IFRS utilisées par d'autres sociétés, ce qui réduit
leur utilité comme mesures financières comparatives. En raison de
ces limites, il est nécessaire de prendre en considération ces
mesures financières ajustées parallèlement aux autres mesures
financières IFRS.
Les articles suivants sont exclus de la perte nette ajustée et
de la perte nette ajustée par action:
Charges liées aux rémunérations en actions: Nous excluons les
charges liées aux rémunérations en action de nos mesures
financières ajustées, car ce type de charge, non monétaire, fluctue
de temps en temps, en raison de facteurs hors de notre contrôle,
tels le cours de notre action à la date d'émission des subventions
en actions. Les charges liées aux rémunérations en actions sont, et
continueront d'être, dans un avenir prévisible, une dépense
récurrente dans le cadre de notre activité et un élément important
de notre stratégie de rémunération.
Certains autres postes: Nous excluons certains autres postes
significatifs susceptibles de se produire occasionnellement et qui
ne constituent pas des dépenses opérationnelles récurrentes
normales, de trésorerie ou hors trésorerie, dans le cadre de nos
mesures financières ajustées. Ce type de poste est évalué au cas
par cas par la direction, sur la base des aspects à la fois
quantitatifs et qualitatifs de leur nature. Ils représentent
généralement des postes qui, soit en résultat de leur nature ou de
leur signification, se produiraient régulièrement dans le cadre de
notre activité normale, sans que la direction ne l'ait prévu. En
contraste, parmi la liste non exhaustive d'exemples de certains
autres postes significatifs exclus de nos mesures financières
ajustées figureraient: les variations de la juste valeur des
instruments dérivés, le gain comptabilisé en lien avec le
décaissement de 50,0 millions USD, la mise en place de l'emprunt
dérivé et résiduel incorporé, l'élimination de l'instrument dérivé
immédiatement avant l'approbation de ZYNLONTA par la FDA, la charge
d'intérêts effective associée à l'accord de facilité conclu avec
Deerfield, les coûts de transaction associés à des émissions de
titres de créances ou d'actions passées en charges en vertu des
IFRS, ainsi que la charge d'intérêts effective associée à une
obligation différée de redevances en vertu de l'accord d'achat de
redevances conclu avec HealthCare Royalty.
Veuillez consulter le rapprochement des mesures IFRS et non IFRS
ci-joint pour toute explication des montants exclus et inclus
aboutissant aux mesures financières non IFRS correspondant aux
périodes de trois et de neuf mois closes aux 30 septembre 2021 et
2020.
Déclarations prospectives
Le présent communiqué de presse contient des déclarations qui
constituent des déclarations prospectives. Toutes les déclarations
autres que les faits historiques contenues dans le présent
communiqué de presse, y compris les déclarations concernant nos
résultats d'exploitation et notre situation financière futurs,
notre stratégie d'entreprise et de commercialisation, nos produits
et produits candidats, notre portefeuille de recherche, les études
précliniques et les essais cliniques en cours et prévus, les
soumissions et approbations réglementaires, les activités
commerciales prévues, les coûts de recherche et de développement,
le calendrier et les perspectives de succès, ainsi que les plans et
objectifs de la direction concernant les activités futures,
constituent des déclarations prospectives. Les déclarations
prospectives sont basées sur les convictions et hypothèses de la
direction et sur les informations dont elle dispose actuellement.
Ces déclarations sont soumises à des risques et des incertitudes,
et les résultats réels pourraient différer sensiblement de ceux
exprimés ou sous-entendus dans les déclarations prospectives en
raison de divers facteurs, y compris ceux décrits dans nos
documents déposés auprès de la Securities and Exchange Commission
américaine. Aucune garantie ne peut être donnée que ces résultats
futurs seront atteints. Ces déclarations prospectives contenues
dans ce document ne sont valables qu’à la date de publication du
présent communiqué de presse. Nous déclinons expressément toute
obligation et tout engagement de mettre à jour ces déclarations
prospectives contenues dans le présent communiqué de presse afin de
refléter tout changement dans nos attentes ou tout changement dans
les événements, conditions ou circonstances sur lesquels ces
déclarations sont basées, sauf si la législation en vigueur
l’exige. Aucune déclaration ou garantie (explicite ou implicite)
n’est faite quant à l’exactitude desdites déclarations
prospectives.
ADC Therapeutics SA
Etat des résultats consolidé
condensé provisoire (non-vérifié)
(en milliers d'USD, à
l'exception des actions et des données par action)
Pour la période de trois mois
close au 30 septembre
Pour la période de neuf
mois close au 30 septembre
2021
2020 (1)
2021
2020 (1)
Vente de produits nette
13.147
-
16.907
-
Frais opérationnels Coût des ventes de produits
(502
)
-
(623
)
-
Dépenses de Recherche et de Développement
(36.805
)
(32.155
)
(115.510
)
(93.480
)
Dépenses de Vente et de Marketing
(17.045
)
(6.116
)
(46.177
)
(12.748
)
Dépenses générales et administratives
(16.587
)
(14.157
)
(53.536
)
(35.034
)
Total dépenses opérationnelles
(70.939
)
(52.428
)
(215.846
)
(141.262
)
Perte d'exploitation
(57.792
)
(52.428
)
(198.939
)
(141.262
)
Autres revenus (charges) Autres (charges) revenus
(203
)
145
190
423
Emprunts convertibles, instruments dérivés, changement des revenus
à la juste valeur (charges)
(6.943
)
33.868
16.279
(45.393
)
Emprunts convertibles, instruments dérivés, coûts de transaction
-
-
(148
)
(1.571
)
Quote-part du résultat des activités de la coentreprise
(2.210
)
-
(3.906
)
-
Revenus financiers
16
163
46
732
Charge financière
(4.265
)
(1.940
)
(8.820
)
(2.879
)
Revenus liés aux écarts de change (perte)
(7
)
(139
)
145
(210
)
Total autres (charges) revenus
(13.612
)
32.097
3.786
(48.898
)
Pertes avant impôts
(71.404
)
(20.331
)
(195.153
)
(190.160
)
Economie d'impôts (charges)
(145
)
3
(492
)
(201
)
Perte nette
(71.549
)
(20.328
)
(195.645
)
(190.361
)
Perte nette attribuable à: Propriétaires de la
société-mère
(71.549
)
(20.328
)
(195.645
)
(190.361
)
Perte nette par action, de base et diluée
(0,93
)
(0,29
)
(2,55
)
(3,09
)
(1) La période précédente a été modifiée
pour conformité aux charges de Ventes et de Marketing, afin que sa
présentation soit conforme à celle de la période courante.
ADC Therapeutics SA
Bilan consolidé condensé
provisoire (non-vérifié)
(en milliers d'USD)
30 septembre2021 31 décembre2020 ACTIFS
Actifs courants Trésorerie et équivalents de trésorerie
530.194
439.195
Comptes débiteurs nets
15.896
-
Stock
8.008
-
Autres actifs courants
14.310
11.255
Total actifs courants
568.408
450.450
Actifs non courants Immobilisations corporelles
4.022
1.629
Droit d'utilisation des actifs
7.540
3.129
Actifs incorporels
13.316
10.179
Participation dans une coentreprise
44.002
47.908
Autres actifs à long terme
691
397
Total actifs non courants
69.571
63.242
Total actifs
637.979
513.692
PASSIF ET CAPITAUX PROPRES Passifs courants
Créance
12.028
5.279
Autres passifs courants
39.685
30.375
Passif de location à court terme
1.012
1.002
Dette d'impôt éligible
-
149
Emprunts convertibles à court terme
6.575
3.631
Total passif courant
59.300
40.436
Passif non-courant Emprunts convertibles à long terme
85.877
34.775
Emprunts convertibles, instruments dérivés
56.562
73.208
Obligation différée de redevances, à long terme
214.629
-
Gain différé en coentreprise
23.539
23.539
Crédits-baux, à long terme
7.183
2.465
Indemnités de départ en retraite
3.581
3.543
Autre passif non-courant
-
221
Total passif non-courant
391.371
137.751
Total passif
450.671
178.187
Capitaux propres attribuables aux propriétaires de la
société-mère Capital social
6.445
6.314
Prime d'émission
981.570
981.056
Actions propres
(133
)
(4
)
Autres réserves
89.769
42.753
Ecart de conversion cumulé
161
245
Pertes cumulées
(890.504
)
(694.859
)
Total capitaux propres attribuables aux propriétaires de la
société-mère
187.308
335.505
Total passif et capitaux propres
637.979
513.692
ADC Therapeutics SA
Rapprochement des mesures IFRS
et non-IFRS (non-vérifié)
(en milliers d'USD, à
l'exception des actions et des données par action)
Période de trois mois close
au
30 septembre
Période de neuf mois close
au
30 septembre
(en milliers d'USD, à l'exception des actions et des données par
action)
2021
2020
2021
2020
Perte nette
(71.549
)
(20.328
)
(195.645
)
(190.361
)
Ajustements: Rémunérations basées sur des actions (i)
14.798
10.988
47.016
27.512
Emprunts convertibles, instruments dérivés, changement de la juste
valeur (ii)
6.943
(33.868
)
(16.279
)
45.393
Emprunts convertibles, première et seconde tranche, instruments
dérivés, coûts de transaction (iii)
-
-
148
1.571
Charge d'intérêts effective (iv)
4.207
1.913
8.639
2.781
Perte nette ajustée
(45.601
)
(41.295
)
(156.121
)
(113.104
)
Perte nette par action, de base et diluée
(0,93
)
(0,29
)
(2,55
)
(3,09
)
Résultat net retraité par action, de base et diluée
0,34
(0,29
)
0,52
1,25
Perte nette ajustée par action, de base et diluée
(0,59
)
(0,58
)
(2,03
)
(1,84
)
Nombre moyen pondéré d'actions en circulation, de base et diluée
76.739.770
70.914.300
76.730.117
61.613.177
(i)
Les rémunérations fondées sur des actions
représentent le coût des attributions en action émises à
l'intention de nos administrateurs, de notre direction et de nos
employés. La juste valeur des attributions est calculée au moment
de l'attribution. Elle est reconnue, lors de la période
d'acquisition des droits d'attribution, par une charge dans le
compte de résultat et une augmentation correspondante dans d'autres
réserves de capitaux. Ces entrées comptables n'ont aucune incidence
sur la trésorerie.
(ii)
Le changement de la juste valeur des
instruments dérivés de l'emprunt convertible résulte de
l'évaluation réalisée à la fin de chaque période comptable des
instruments dérivés associés aux emprunts convertibles, ainsi que
du gain comptabilisé en lien avec la réception des 50,0 millions
USD, de la mise en place de l'emprunt dérivé et résiduel incorporé
associé à la facilité de crédit convertible Deerfield et de
l'élimination de l'instrument dérivé immédiatement avant
l'approbation du ZYNLONTA par la FDA lors du second trimestre 2021,
comme expliqué en note 13 "Billets convertibles" de l'état
financier condensé consolidé provisoire. Ces évaluations comportent
plusieurs données. Les variations de la valeur de l'instrument
sous-jacent (c'est-à-dire des changements du prix de nos actions
ordinaires) et des changements en termes de volatilité attendue
dudit prix sont celles les plus susceptibles d'entraîner
d'importants changements lors des évaluations. Ces entrées
comptables n'ont aucune incidence sur la trésorerie.
(iii)
Les coûts de transaction attribués aux
instruments dérivés de la première et seconde tranche de l'emprunt
convertible représentent les coûts réels. Ceux-ci ne devraient pas
se reproduire de façon continue.
(iv)
La charge d'intérêts effective se rapporte
à l'augmentation de la valeur de nos emprunts convertibles et
obligations différées de redevances, selon les termes de l'accord
d'achat de redevances conclu avec HCR conformément à la méthode du
taux d'intérêt effectif. Veuillez consulter les notes 13 "Emprunts
convertibles" et 15 "Obligation différée de redevances" de l'état
financier consolidé condensé provisoire.
Le texte du communiqué issu d’une traduction ne doit d’aucune
manière être considéré comme officiel. La seule version du
communiqué qui fasse foi est celle du communiqué dans sa langue
d’origine. La traduction devra toujours être confrontée au texte
source, qui fera jurisprudence.
Consultez la
version source sur businesswire.com : https://www.businesswire.com/news/home/20211103005502/fr/
Investisseurs Eugenia Litz ADC Therapeutics
Eugenia.Litz@adctherapeutics.com +44 7879 627205 Amanda Hamilton
ADC Therapeutics amanda.hamilton@adctherapeutics.com Tél.: +1
917-288-7023 Médias des Etats-Unis Mary Ann Ondish ADC
Therapeutics maryann.ondish@adctherapeutics.com Tél.: +1
914-552-4625 Médias de l'UE Alexandre Müller Dynamics Group
amu@dynamicsgroup.ch Tél.: +41 (0) 43 268 3231
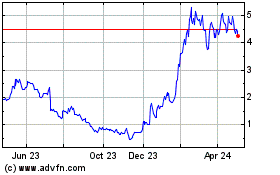
ADC Therapeutics (NYSE:ADCT)
Historical Stock Chart
From Aug 2024 to Sep 2024
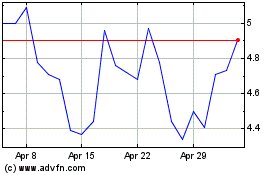
ADC Therapeutics (NYSE:ADCT)
Historical Stock Chart
From Sep 2023 to Sep 2024