ADC Therapeutics: Auf der 16. jährlichen International Conference on Malignant Lymphoma wurden vielversprechende Zwischenerg...
June 22 2021 - 11:08PM
Business Wire
Dosierungsschema aus der Phase-2-Studie führt
zu ermutigender Gesamtansprechrate und lang anhaltenden
Behandlungseffekten bei stark vorbehandelten Patienten mit
rezidiviertem oder refraktärem Hodgkin-Lymphom
Sicherheitsprofil der Phase 2 konsistent mit
Phase 1 – auch in Bezug auf die GBS-Inzidenz
ADC Therapeutics SA (NYSE: ADCT), ein kommerziell tätiges
Biotechnologieunternehmen, das in der Entwicklung neuartiger
Antik�rper-Wirkstoff-Konjugate (AWK) zur Behandlung hämatologischer
Malignome und solider Tumore führend ist, gab heute bekannt, dass
auf der 16. jährlichen International Conference on Malignant
Lymphoma (ICML) aktualisierte Zwischenergebnisse der laufenden
zulassungsrelevanten klinischen Phase-2-Studie mit
Camidanlumab-Tesirin (Cami) an Patienten mit rezidiviertem oder
refraktärem Hodgkin-Lymphom im Rahmen eines mündlichen Vortrags
(Abstract 075) vorgestellt wurden. Die Daten der
zulassungsrelevanten Phase-2-Studie sollen den
Biologika-Zulassungsantrag (Biologics License Application)
unterstützen.
„Die Zwischenergebnisse aus unserer laufenden
zulassungsrelevanten Phase-2-Studie mit Cami als Monotherapie für
Patienten mit rezidiviertem oder refraktärem Hodgkin-Lymphom haben
lang anhaltende Behandlungseffekte bei einer beträchtlichen Zahl
von Patienten gezeigt“, so Jay Feingold, MD, PhD, Senior Vice
President und Chief Medical Officer von ADC Therapeutics. „In Phase
2 haben wir das in Phase 1 ermittelte optimale Dosierungsschema
basierend auf Aktivität und Verträglichkeit verwendet. Die
Zwischenergebnisse, denen zufolge die mediane Ansprechdauer nicht
erreicht wurde, sind ermutigend. Zudem haben wir festgestellt, dass
die GBS-Inzidenz konsistent mit Phase 1 ist. Wir werden aktuelle
Informationen zu diesem zulassungsrelevanten Programm präsentieren,
sobald uns weitere Daten zur Gesamtansprechrate und Ansprechdauer
vorliegen.“
Derzeit wird Cami in einer multizentrischen, offenen, einarmigen
klinischen Phase-2-Studie an 117 Patienten mit rezidiviertem oder
refraktärem Hodgkin-Lymphom untersucht, bei denen zuvor ≥3
Behandlungslinien angewendet wurden (≥2 Linien, falls sie für eine
hämatopoetische Stammzelltransplantation, HSZT, nicht geeignet
sind), einschließlich einer vorherigen Behandlung mit Brentuximab
Vedotin und einem Checkpoint-Inhibitor. Die vorläufigen Daten
umfassen 101 auswertbare Patienten mit einer medianen
Teilnahmedauer an der Studie von 5,1 Monaten. Bei den stark
vorbehandelten Patienten wurden im Median zuvor 6 systemische
Therapielinien angewendet.
Zu den wichtigsten Daten, die Pier Luigi Zinzani, MD, PhD, IRCCS
Azienda Ospedaliero-Universitaria di Bologna Istituto di Ematologia
„Seràgnoli“, und Dipartimento di Medicina Specialistica,
Diagnostica e Sperimentale Università di Bologna, Bologna, Italien,
auf der ICML vorgestellt hat, geh�ren:
- Die Gesamtansprechrate (ORR) betrug 66,3 % (67/101
Patienten) bei einer kompletten Ansprechrate (CRR) von 27,7 %
und einer partiellen Ansprechrate (PRR) von 38,6 %
- Die mediane Ansprechdauer wurde nicht erreicht
- Es wurden keine neuen Sicherheitssignale erkannt. Die
häufigsten therapiebedingten unerwünschten Ereignisse dritten oder
h�heren Grades bei ≥5 % der Patienten waren Hypophosphatämie
(7,7 %), makulopapul�ser Ausschlag (6,8 %),
Thrombozytopenie (6,8 %), Anämie (6,0 %) und Lymphopenie
(6,0 %)
- Bislang konnten neun Patienten (7,7 %) nach der
Cami-Behandlung mit einer HSZT fortfahren
- 7/117 Patienten (6,0 %) entwickelten ein
Guillain-Barre-Syndrom/Polyradikulopathie (konsistent mit der
Inzidenz bei den Hodgkin-Lymphom-Patienten aus Phase 1)
„Für Patienten mit rezidiviertem oder refraktärem
Hodgkin-Lymphom, die zuvor auf mehrere Therapielinien wie
Brentuximab Vedotin und eine PD-1-Blockade nicht angesprochen
haben, bestehen nur begrenzte Behandlungsm�glichkeiten“, berichtet
Dr. Zinzani. „Die Antitumoraktivität und das Sicherheitsprofil von
Cami demonstrieren weiterhin das Potenzial dieses neuartigen, auf
CD25 zielenden AWK, den ungedeckten Bedarf bei stark vorbehandelten
Patienten decken zu k�nnen.“
Über Camidanlumab-Tesirin (Cami)
Camidanlumab-Tesirin (Cami, vormals ADCT-301) ist ein
Antik�rper-Wirkstoff-Konjugat (AWK), das aus einem monoklonalen
Antik�rper besteht, der an CD25 (HuMax®-TAC, lizenziert von Genmab
A/S) bindet und mit der Pyrrolobenzodiazepin (PBD)-Dimer-Nutzlast
Tesirin konjugiert ist. Einmal an eine CD25-exprimierende
Tumorzelle gebunden wird Cami in die Zelle internalisiert, wo
Enzyme den PBD-basierten Sprengkopf freisetzen und die Zelle
abt�ten. Dies gilt sowohl für CD25-exprimierende Tumorzellen als
auch für CD25-exprimierende Tregs. Die intratumorale Freisetzung
des PBD-Sprengkopfes kann auch zum „Bystander-Killing“ benachbarter
Tumorzellen führen. Außerdem hat sich gezeigt, dass PBDs den
immunogenen Zelltod induzieren. Alle diese Eigenschaften von Cami
k�nnen die immunvermittelte Anti-Tumor-Aktivität verbessern.
Cami wird in einer zulassungsrelevanten klinischen
Phase-2-Studie an Patienten mit rezidiviertem oder refraktärem
Hodgkin-Lymphom (HL) sowie in einer klinischen Phase-1b-Studie als
Monotherapie und in Kombination mit Pembrolizumab bei soliden
Tumoren untersucht.
Über ADC Therapeutics
ADC Therapeutics (NYSE: ADCT) ist ein kommerziell tätiges
Biotechnologieunternehmen, das mit seinen zielgerichteten
Antik�rper-Wirkstoff-Konjugaten (AWK) der nächsten Generation die
Lebensqualität von Krebspatienten verbessert. Das Unternehmen
treibt die Entwicklung seiner proprietären PBD-basierten
AWK-Technologie voran, um das Behandlungsparadigma für Patienten
mit hämatologischen Malignomen und soliden Tumoren zu
verändern.
Das auf CD19 abzielende AWK ZYNLONTA™
(Loncastuximab-Tesirin-Lpyl) ist von der FDA für die Behandlung des
rezidivierten oder refraktären diffusen großzelligen
B-Zell-Lymphoms nach zwei oder mehr Linien systemischer Therapie
zugelassen. Auch in Kombination mit anderen Wirkstoffen wird
ZYNLONTA in fortgeschrittenen klinischen Studien geprüft. Cami
(Camidanlumab-Tesirin) wird in einer späten klinischen Studie bei
rezidiviertem oder refraktärem Hodgkin-Lymphom und in einer
klinischen Phase-1b-Studie bei verschiedenen fortgeschrittenen
soliden Tumoren geprüft. Neben ZYNLONTA und Cami hat das
Unternehmen mehrere PBD-basierte AWK in laufender klinischer und
präklinischer Entwicklung.
ADC Therapeutics hat seinen Sitz in Lausanne (Biopôle), Schweiz,
und unterhält Niederlassungen in London, der San Francisco Bay Area
und New Jersey. Für weitere Informationen besuchen Sie
https://adctherapeutics.com/. Folgen Sie dem Unternehmen auf
Twitter und LinkedIn.
ZYNLONTA™ ist eine Marke von ADC Therapeutics SA.
Die Ausgangssprache, in der der Originaltext ver�ffentlicht
wird, ist die offizielle und autorisierte Version. Übersetzungen
werden zur besseren Verständigung mitgeliefert. Nur die
Sprachversion, die im Original ver�ffentlicht wurde, ist
rechtsgültig. Gleichen Sie deshalb Übersetzungen mit der originalen
Sprachversion der Ver�ffentlichung ab.
Originalversion auf businesswire.com
ansehen: https://www.businesswire.com/news/home/20210622006150/de/
Investoren Eugenia Litz ADC Therapeutics
Eugenia.Litz@adctherapeutics.com +44 7879 627205
Amanda Hamilton ADC Therapeutics
amanda.hamilton@adctherapeutics.com +1 917-288-7023
EU-Medien Alexandre Müller Dynamics Group amu@dynamicsgroup.ch
+41 (0) 43 268 3231
US-Medien Annie Starr 6 Degrees astarr@6degreespr.com +1
973-768-2170
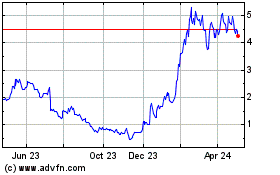
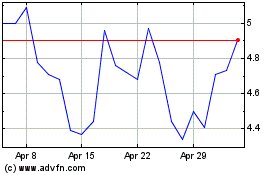
ADC Therapeutics (NYSE:ADCT)
Historical Stock Chart
From Mar 2024 to Apr 2024
ADC Therapeutics (NYSE:ADCT)
Historical Stock Chart
From Apr 2023 to Apr 2024